Мирошниченко Ольга: "Исследование влияния -ОН группы на структуру и электрические свойства нанокластеров оксида титана" — различия между версиями
| (не показаны 3 промежуточные версии этого же участника) | |||
| Строка 2: | Строка 2: | ||
Оксид титана (TiO2) - полупроводник с широкой запрещенной зоной, имеющий огромное количество применений. Обычно его используют в качестве белого пигмента и фотокатализатора. В силу его безвредности, TiO2 применяют в фармакологии, пищевой промышленности, а также в медицинских и стоматологических имплантатах и в качестве УФ-блокиратора. Свойства оксида титана определяются его механической и электронной структурой, на которые большое влияние оказывают различные адсорбаты. Гидроксильные группы (-ОН) всегда присутствуют на поверхности оксида титана, поэтому исследование влияния –ОН группы на свойства полупроводника крайне важно. | Оксид титана (TiO2) - полупроводник с широкой запрещенной зоной, имеющий огромное количество применений. Обычно его используют в качестве белого пигмента и фотокатализатора. В силу его безвредности, TiO2 применяют в фармакологии, пищевой промышленности, а также в медицинских и стоматологических имплантатах и в качестве УФ-блокиратора. Свойства оксида титана определяются его механической и электронной структурой, на которые большое влияние оказывают различные адсорбаты. Гидроксильные группы (-ОН) всегда присутствуют на поверхности оксида титана, поэтому исследование влияния –ОН группы на свойства полупроводника крайне важно. | ||
| − | В данной работе рассмотрены два (TiO2)16 нанокластера анатаза (структуры А и Б), одной из трех полиморфных модификаций оксида титана, наиболее устойчивой в случае наноструктур. Целью работы является провести ab initio расчеты для кластеров оксида титана, с присоединенной группой -ОН и выявить влияние гидроксильной группы на свойства TiO2. | + | В данной работе рассмотрены два (TiO2)16 нанокластера анатаза (структуры А и Б), одной из трех полиморфных модификаций оксида титана, наиболее устойчивой в случае наноструктур. Целью работы является провести ''ab initio'' расчеты для кластеров оксида титана, с присоединенной группой -ОН и выявить влияние гидроксильной группы на свойства TiO2. |
== Результаты == | == Результаты == | ||
| − | + | 1. Рассмотрены 2 структуры (А и Б), вырезанные из большого объема. На поверхности второй имеются низкокоординированные атомы кислорода. | |
| − | На поверхности второй имеются низкокоординированные атомы кислорода. | + | <gallery caption="Кластеры до релаксации" widths="250px" heights="250px"> |
| + | Файл:an16ndbur.jpg|Структура А | ||
| + | Файл:an16dbur.jpg|Структура Б | ||
| + | </gallery> | ||
| − | + | 2. Структуры были оптимизированы квази-Ньютоновским методом с использованием программного пакета [https://wiki.fysik.dtu.dk/gpaw/ GPAW]. Условие сходимости: силы на всех атомах должны быть меньше 0.01 еВ. | |
| + | <gallery caption="Кластеры после релаксации" widths="250px" heights="250px"> | ||
| + | Файл:Anatase16ndb.jpg|Структура А | ||
| + | Файл:Anatase16db.jpg|Структура Б | ||
| + | </gallery> | ||
| − | |||
| − | + | 3. Были проведены тестовые расчеты, и найдены атомы титана в обеих конструкциях, к которым была присоединена -ОН группа. Полученные структуры также были оптимизированы. | |
| + | <gallery caption="Кластеры после релаксации, с присоединенной -ОН" widths="250px" heights="250px"> | ||
| + | Файл:Anatase16ndbOH.jpg|Структура А | ||
| + | Файл:Anatase16dbOH.jpg|Структура Б | ||
| + | </gallery> | ||
| − | + | 4. Было подсчитано количество, средние длины связей, размеры кластеров и проведено сравнение результатов для структур с группой ОН до и после релаксации. | |
| − | ** Средняя длина связей в обеих структурах стала на 0.5% короче | + | * В обеих структурах была прервана связь между атомом титана, к которому была присоединена группа ОН, и нижним атомом кислорода. В структуре Б больше прерванных Ti-O связей, в структуре А обрывается связь Ti-Ti, а во второй структуре образовывается новая Ti-Ti связь |
| − | + | * Средняя длина связей в обеих структурах стала на 0.5% короче | |
| − | + | * Связь между кислородом и водородом в гидроксильной группе уменьшилась на 3%, | |
| + | * Связь между атомом титана и группой ОН стала короче на 6%,в структуре А и на 0.5% в Б | ||
=>Структуры стали более компактными | =>Структуры стали более компактными | ||
| − | + | ||
| − | + | * Расширение кластеров в направлении x: A - 7%, Б - 8% | |
| − | + | * Расширение кластеров в направлении z: A - 17%, Б - 19% | |
| + | * Сужение в y-направлении: A - 4.5%, Б - 10% | ||
=> ОН группа вытягивает структуры | => ОН группа вытягивает структуры | ||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| + | 5. Были построены графики плотности состояний (Density of States (DOS)). | ||
| + | <gallery caption="Графики плотности состояний (DOS) для кластеров с группой -ОН и без" widths="250px" heights="250px"> | ||
| + | Файл:dos_ndb_ndbOH.jpg|Структура А | ||
| + | Файл:dos_db_dbOH.jpg|Структура Б | ||
| + | </gallery> | ||
| + | * После присоединения гидроксильной группы ширина зоны между Высшей Занятой Молекулярной Орбиталью (ВЗМО) и Низшей Свободной Молекулярной Орбиталью (НСМО) стала практически равной нулю, что свидетельствует об уменьшении границы поглощения | ||
| + | *Уменьшение границы поглощения означает, что материал становится более эффективен в фотокатализе и очистке воды. Частицы становятся менее прозрачными. | ||
| + | *Стабилизируется электронная структура в случае кластера Б, что означает большую устойчивость и прочность материала | ||
| + | |||
[[Category: Студенческие проекты]] | [[Category: Студенческие проекты]] | ||
Текущая версия на 02:43, 28 июня 2012
Актуальность[править]
Оксид титана (TiO2) - полупроводник с широкой запрещенной зоной, имеющий огромное количество применений. Обычно его используют в качестве белого пигмента и фотокатализатора. В силу его безвредности, TiO2 применяют в фармакологии, пищевой промышленности, а также в медицинских и стоматологических имплантатах и в качестве УФ-блокиратора. Свойства оксида титана определяются его механической и электронной структурой, на которые большое влияние оказывают различные адсорбаты. Гидроксильные группы (-ОН) всегда присутствуют на поверхности оксида титана, поэтому исследование влияния –ОН группы на свойства полупроводника крайне важно.
В данной работе рассмотрены два (TiO2)16 нанокластера анатаза (структуры А и Б), одной из трех полиморфных модификаций оксида титана, наиболее устойчивой в случае наноструктур. Целью работы является провести ab initio расчеты для кластеров оксида титана, с присоединенной группой -ОН и выявить влияние гидроксильной группы на свойства TiO2.
Результаты[править]
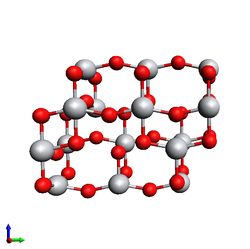
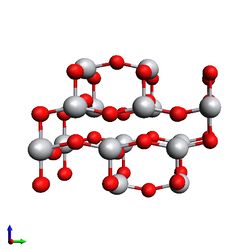
1. Рассмотрены 2 структуры (А и Б), вырезанные из большого объема. На поверхности второй имеются низкокоординированные атомы кислорода.
- Кластеры до релаксации
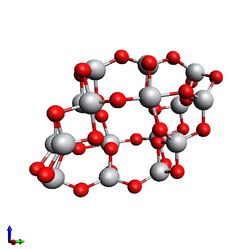
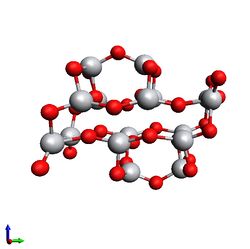
2. Структуры были оптимизированы квази-Ньютоновским методом с использованием программного пакета GPAW. Условие сходимости: силы на всех атомах должны быть меньше 0.01 еВ.
- Кластеры после релаксации
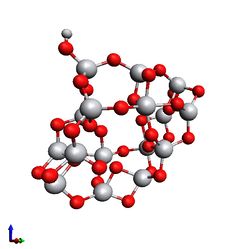
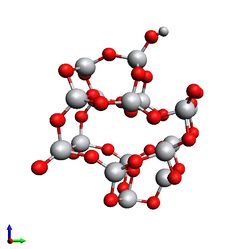
3. Были проведены тестовые расчеты, и найдены атомы титана в обеих конструкциях, к которым была присоединена -ОН группа. Полученные структуры также были оптимизированы.
- Кластеры после релаксации, с присоединенной -ОН
4. Было подсчитано количество, средние длины связей, размеры кластеров и проведено сравнение результатов для структур с группой ОН до и после релаксации.
- В обеих структурах была прервана связь между атомом титана, к которому была присоединена группа ОН, и нижним атомом кислорода. В структуре Б больше прерванных Ti-O связей, в структуре А обрывается связь Ti-Ti, а во второй структуре образовывается новая Ti-Ti связь
- Средняя длина связей в обеих структурах стала на 0.5% короче
- Связь между кислородом и водородом в гидроксильной группе уменьшилась на 3%,
- Связь между атомом титана и группой ОН стала короче на 6%,в структуре А и на 0.5% в Б
=>Структуры стали более компактными
- Расширение кластеров в направлении x: A - 7%, Б - 8%
- Расширение кластеров в направлении z: A - 17%, Б - 19%
- Сужение в y-направлении: A - 4.5%, Б - 10%
=> ОН группа вытягивает структуры
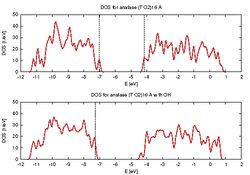
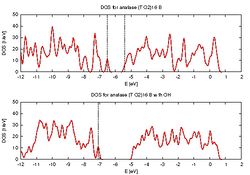
5. Были построены графики плотности состояний (Density of States (DOS)).
- Графики плотности состояний (DOS) для кластеров с группой -ОН и без
- После присоединения гидроксильной группы ширина зоны между Высшей Занятой Молекулярной Орбиталью (ВЗМО) и Низшей Свободной Молекулярной Орбиталью (НСМО) стала практически равной нулю, что свидетельствует об уменьшении границы поглощения
- Уменьшение границы поглощения означает, что материал становится более эффективен в фотокатализе и очистке воды. Частицы становятся менее прозрачными.
- Стабилизируется электронная структура в случае кластера Б, что означает большую устойчивость и прочность материала